
PRUEBAS BIOMÉDICAS
Instron aporta una gran cantidad de conocimientos a la industria biomédica, sirviendo como socio estratégico para empresas de todos los tamaños. Nuestros equipos y servicios están preparados para ayudarle a investigar nuevas tecnologías y garantizar la calidad del producto, todo ello manteniendo los más altos niveles de integridad y seguridad de los datos. Al estar integrados en la industria biomédica durante más de 75 años, los desafíos tecnológicos, normativos y de fabricación a los que se enfrentan nuestros clientes nos han llevado a desarrollar productos y servicios para satisfacer sus necesidades. Estos desarrollos incluyen accesorios especializados, software compatible y capacidades de automatización. Nuestro activo más valioso es nuestra amplia red de clientes, que representa una amplia gama de fabricantes de dispositivos médicos y farmacéuticos, CDMO, universidades, casas de pruebas y startups.
Nuestros clientes están a la vanguardia de la innovación tecnológica médica, trabajando para mejorar los resultados de los pacientes mediante el desarrollo de productos nuevos y mejores. Estas empresas están aumentando la eficacia de los tratamientos mínimamente invasivos, desarrollando la próxima generación de sensores portátiles y reinventando un futuro en el que los robots quirúrgicos son habituales en el quirófano. En cada caso, Instron ha ayudado a crear un sólido programa de pruebas mecánicas capaz de cumplir los requisitos y superar los obstáculos de cada paso del proceso de desarrollo del producto.

La gama de aplicaciones biomédicas abarca una amplia gama de áreas terapéuticas, aportando una gama extremadamente amplia de requisitos de pruebas. Se deben añadir varias disposiciones de utillaje a un sistema de análisis universal para sostener o manipular correctamente las muestras de análisis y obtener los resultados necesarios. En muchos casos, los estándares internacionales como ISO o ASTM impulsan el diseño definitivo de estos accesorios. Como alternativa, muchos están diseñados específicamente para las especificaciones del dispositivo del cliente. Nuestra experiencia en la industria ha ayudado a crear un catálogo de empuñaduras y accesorios para adaptarse a los dispositivos más comunes y cumplir con los estándares más utilizados. Nuestro grupo de soluciones de ingeniería está disponible para trabajar con usted para desarrollar accesorios específicos para sus necesidades.


APLICACIÓN DE TENDENCIAS
PRUEBA DE DISPOSITIVOS PORTÁTILES
Las tendencias en la tecnología portátil siguen a las de los – dispositivos de la industria biomédica y electrónica en general, cada vez más pequeños, inteligentes y fáciles de usar. Los dispositivos portátiles en el sector sanitario han pasado a soluciones que reducen el perfil del dispositivo, proporcionan más integración con las aplicaciones de los teléfonos inteligentes y, lo que es más importante, permiten a los pacientes recibir sus tratamientos en casa en lugar de en la consulta de un médico. A medida que esta tendencia continúa, los fabricantes están trabajando para desarrollar métodos de prueba robustos para evaluar mecánicamente todos los aspectos de estos dispositivos y garantizar que funcionan según lo esperado. Además de probar los componentes del dispositivo de inyección, los fabricantes también se enfrentan a desafíos a la hora de evaluar y seleccionar los adhesivos para estos productos.
La industria farmacéutica se basa en pruebas mecánicas para evaluar los sistemas de administración de fármacos y sus envases asociados. Los sistemas de administración de fármacos pueden utilizar vías dérmicas, subcutáneas, intramusculares, orales o nasales y vienen en una variedad de formatos de envase diferentes. Los sistemas de pruebas universales se utilizan durante todo el proceso de desarrollo del producto para ayudar a identificar los materiales adecuados, evaluar los mecanismos de entrega, realizar la validación del diseño, validar los procesos de fabricación y permitir medidas de control de calidad adecuadas. Las aplicaciones más comunes están relacionadas con sistemas de inyección basados en agujas e implican pruebas funcionales basadas en estándares del sector como ISO 11040 e ISO 11608 o pruebas de usabilidad de productos para complementar las pruebas de factores humanos.
Los consumibles médicos representan la subsección más grande de las pruebas biomédicas e incluyen una amplia variedad de productos de un solo uso como herramientas quirúrgicas, EPP, productos de cierre de heridas, productos de recogida de muestras y más. Estos productos son normalmente dispositivos médicos de clase I o II de la FDA, que, a pesar de tener requisitos de prueba menos estrictos, se producen en cantidades tan grandes que se debe tener cuidado para acomodar las pruebas de alto volumen. Para compensar los volúmenes más grandes, el rendimiento y la repetibilidad se convierten en requisitos de prueba críticos, abordados a través de utillaje especializado, flujos de trabajo eficientes del operador y software intuitivo.
Tanto con fines diagnósticos como terapéuticos, el mercado de dispositivos vasculares intervencionistas ha crecido de forma exponencial. Los productos como las guías y los catéteres son esenciales para el mapeo de la vasculatura, la eliminación de bloqueos y la colocación de stents o implantes. La evaluación de las propiedades del material y del revestimiento de estos productos es esencial para garantizar que funcionen como se espera en vivo. Las pruebas in vitro también pueden realizarse mediante sistemas llave en mano construidos para imitar las condiciones del mundo real con modelos anatómicos, midiendo las fuerzas relacionadas con el despliegue y la retirada de estos dispositivos. Los dispositivos implantados, como las válvulas de repuesto y los stents, también se someten a pruebas de durabilidad a largo plazo utilizando sistemas dinámicos para validar las respuestas a largo plazo de estos productos a las condiciones del cuerpo.
Los materiales biológicos incluyen los materiales que se encuentran en la naturaleza, el cuerpo humano y otras especies animales. Estos materiales pueden ser tejidos duros, como hueso o esmalte dental, o blandos, como tendones y ligamentos. La variación biológica y los factores ambientales afectan las propiedades mecánicas de estos materiales. También son anisotrópicos y no homogéneos, lo que los convierte en materiales difíciles de recrear o diseñar fuera de la naturaleza.
Los implantes ortopédicos son implantes que soportan el sistema esquelético. Estos incluyen tornillos óseos, placas, barras y clavos para la reparación de fracturas, así como caderas, rodillas y componentes espinales artificiales completos. Los implantes ortopédicos pueden insertarse temporalmente en el cuerpo para ayudar a la cicatrización del paciente, o pueden insertarse en el cuerpo con la intención de que el implante sobreviva al paciente. Dependiendo de su uso, la FDA suele considerar que los implantes ortopédicos son dispositivos médicos de Clase II o Clase III y requieren un rango y una combinación de pruebas mecánicas estáticas y de fatiga.
Los materiales dentales suelen estar compuestos de metal, elastómeros y polímeros. Los dispositivos restauradores y de prostodoncia suelen estar compuestos por múltiples materiales que requieren pruebas mecánicas para determinar cómo interactúan estos materiales para formar el dispositivo terminado. Un implante dental es un poste metálico, normalmente de titanio, que sustituye a todo el diente del paciente. Las pruebas de fatiga representan la forma más común de pruebas mecánicas realizadas en implantes dentales, siguiendo las normas internacionales para evaluar el desgaste esperado del uso repetido.
INTEGRIDAD Y VALIDACIÓN DE DATOS
El concepto de integridad de los datos es fundamental para la fabricación de productos biomédicos e impulsa los programas de calidad que garantizan la seguridad del producto. A nivel mundial, existen numerosos marcos normativos que tienen como objetivo definir qué es la integridad de los datos y cómo debe garantizarse, ya sea dictado por la FDA, las BPF u otros organismos nacionales o internacionales.
Cumplimiento normativo
Dentro de la industria biomédica hay organismos reguladores nacionales e internacionales que definen los protocolos necesarios para garantizar que la seguridad del paciente sea el centro del desarrollo y la fabricación del producto. Organizaciones como la FDA y el MDR de la UE exigen estrictos procesos de control de calidad e integridad de datos. Nuestro paquete de software y productos de servicio permite a los clientes mantener mejor el cumplimiento de sus programas de pruebas mecánicas.
Servicios de validación IQOQ
Nuestros equipos de servicio de campo proporcionan servicios de validación y documentación para respaldar los procesos IQOQ diseñados para garantizar que su equipo de pruebas Instron funcione según sus propósitos previstos y produzca resultados válidos según 21 CFR 820.72 e ISO 13845. Al finalizar nuestros servicios, proporcionamos un certificado de finalización para la instalación y cualificación operativa que será firmado por el ingeniero de servicio de campo de Instron que realizó las validaciones.
Bluehill Central
El software Bluehill Central es una herramienta de gestión de laboratorio que permite la gestión centralizada y remota de las aplicaciones de software Bluehill Universal asociadas a múltiples marcos de ensayo Instron. El software le permite gestionar de forma remota todos los usuarios de Bluehill Universal, las plantillas de ensayo, los resultados, las aprobaciones de las revisiones de los archivos y los datos del registro de auditoría de varios sistemas Instron.
Trazabilidad
El módulo de trazabilidad de Bluehill Universals permite a los usuarios cumplir los requisitos de auditoría asociados a la norma FDA 21 CFR Parte 11, así como los de ISO 17025, Nadcap y otros organismos reguladores. Gracias a la perfecta integración de las aprobaciones electrónicas, el historial de revisiones y una pista de auditoría automatizada, este potente complemento se combina con la seguridad incorporada de Bluehills para ofrecer una trazabilidad de los datos inigualable.

La automatización representa una oportunidad de crecimiento en una variedad de aplicaciones y a lo largo de todo el proceso de desarrollo de productos. En los laboratorios de control de calidad de volumen pequeño y medio, los problemas de rotación del operador y las dificultades de contratación están impulsando la adopción de tecnología de automatización como cobots y etapas XY para mejorar la eficiencia del laboratorio. Incluso dentro de los laboratorios de I+&D o de verificación de dispositivos, la automatización puede garantizar que los ingenieros de pruebas y otros empleados cualificados puedan centrar su tiempo en actividades de valor añadido en lugar de en pruebas manuales. A medida que las empresas pasan a la producción de dispositivos, la realización de pruebas mecánicas completas en línea es un factor fundamental para mejorar el control de los procesos de fabricación y reducir el desperdicio de material o los productos defectuosos. Cada instancia de adición de automatización tiene el potencial de mejorar la eficiencia del laboratorio, reducir la variabilidad y simplificar los procedimientos de prueba.
SISTEMAS DE PRUEBA RECOMENDADOS
Etapa XY automatizada AT2 para sistemas de pruebas universales
El sistema automatizado XY puede realizar pruebas de compresión, flexión o tensión en múltiples componentes o múltiples ubicaciones en un solo dispositivo dentro de una única configuración de prueba para mejorar la eficiencia de las pruebas.

Sistema de ensayo ElectroPuls de 16 estaciones
El sistema de pruebas ElectroPuls 16-Station, utilizado habitualmente para pruebas in vitro de componentes de stent vasculares, realiza pruebas de fatiga de ciclo muy alto en hasta 16 muestras simultáneamente, con una celda de carga con clasificación de fatiga y un ajuste de precisión para cada una.

Sistema de pruebas con agujas curvas
El dispositivo de ensayo de punzonado de aguja curvada se utiliza para evaluar la nitidez de la aguja y la fuerza de inserción; el dispositivo de prueba de doblado de aguja se utiliza para evaluar las propiedades de flexión de la aguja durante su uso.

Sistema de prueba de impacto con impacto de caída de peso
Diseñados para determinar las características de rendimiento de impacto, nuestros sistemas de pruebas de impacto de peso de gota proporcionan un entorno de pruebas simplificado tanto si se analizan muestras como productos finales.






 ISO 7886-1 Pruebas de jeringas hipodérmicas estériles
ISO 7886-1 Pruebas de jeringas hipodérmicas estériles ISO 11040: diseño y propiedades funcionales de las jeringas precargadas
ISO 11040: diseño y propiedades funcionales de las jeringas precargadas ISO 80369: conectores de pequeño calibre para líquidos
ISO 80369: conectores de pequeño calibre para líquidos Prueba de aguja de jeringa
Prueba de aguja de jeringa ISO 11608-1: 2022 Sistemas de inyección basados en agujas
ISO 11608-1: 2022 Sistemas de inyección basados en agujas Ensayo de fuerza de sellado residual (RSF)
Ensayo de fuerza de sellado residual (RSF) Impacto en el rendimiento de las tabletas farmacéuticas
Impacto en el rendimiento de las tabletas farmacéuticas ASTM D7860 Retención de torsión para embalaje a prueba de niños
ASTM D7860 Retención de torsión para embalaje a prueba de niños Pruebas de EPP: incluidas mascarillas, guantes y torundas nasales
Pruebas de EPP: incluidas mascarillas, guantes y torundas nasales Resistencia del sello ASTM F88 de materiales de barrera flexibles
Resistencia del sello ASTM F88 de materiales de barrera flexibles Prueba de aguja curvada según ASTM F3014
Prueba de aguja curvada según ASTM F3014 EN455-2, ISO 11193, ASTM D6319 Pruebas de tracción de guantes médicos
EN455-2, ISO 11193, ASTM D6319 Pruebas de tracción de guantes médicos Pruebas de tensión de suturas quirúrgicas
Pruebas de tensión de suturas quirúrgicas Prueba de stent
Prueba de stent Materiales y estructuras del stent para pruebas de fatiga
Materiales y estructuras del stent para pruebas de fatiga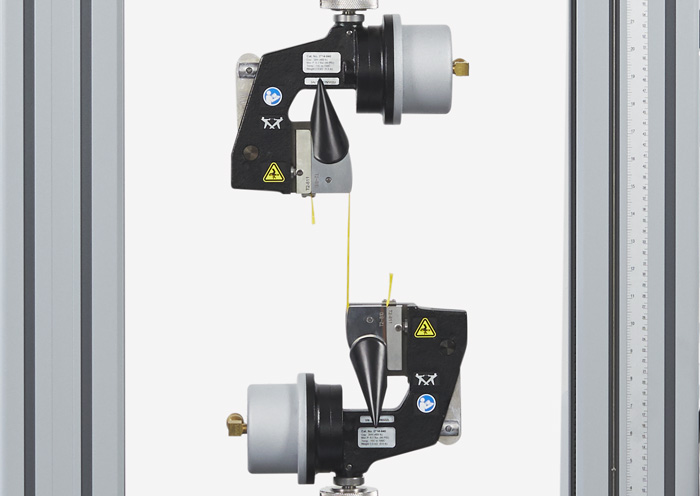 Prueba de tracción ISO 10555 de los tubos del catéter
Prueba de tracción ISO 10555 de los tubos del catéter Prueba de alambre guía
Prueba de alambre guía ASTM F2458 Resistencia al cierre de heridas de adhesivos y selladores tisulares
ASTM F2458 Resistencia al cierre de heridas de adhesivos y selladores tisulares Propiedades de resistencia de los adhesivos tisulares según ASTM F2256 mediante pruebas de pela en T
Propiedades de resistencia de los adhesivos tisulares según ASTM F2256 mediante pruebas de pela en T Prueba de hidrogeles de polímero según ASTM F2150
Prueba de hidrogeles de polímero según ASTM F2150 Análisis de tejidos duros
Análisis de tejidos duros Análisis de tejidos blandos
Análisis de tejidos blandos ASTM F543 - Pruebas axiales y torsionales de tornillos óseos médicos metálicos
ASTM F543 - Pruebas axiales y torsionales de tornillos óseos médicos metálicos Prueba de fatiga cíclica de los constructos de implantes espinales de acuerdo con ASTM F1717-18, ASTM F2706-18 e ISO 12189-8
Prueba de fatiga cíclica de los constructos de implantes espinales de acuerdo con ASTM F1717-18, ASTM F2706-18 e ISO 12189-8 Prueba de fatiga cíclica de prótesis de implante de cadera artificial de acuerdo con las normas ISO 7206-4, ISO 7206-6, ISO-7206-8 y ASTM F2068
Prueba de fatiga cíclica de prótesis de implante de cadera artificial de acuerdo con las normas ISO 7206-4, ISO 7206-6, ISO-7206-8 y ASTM F2068 Prueba de dispositivos de fijación de fracturas
Prueba de dispositivos de fijación de fracturas ASTM F2077 Caracterización y fatiga de los dispositivos de fusión de cuerpos intervertebrales espinales
ASTM F2077 Caracterización y fatiga de los dispositivos de fusión de cuerpos intervertebrales espinales ASTM F2267 Evaluación de dispositivos de fusión de cuerpos intervertebrales vertebrales bajo carga axial
ASTM F2267 Evaluación de dispositivos de fusión de cuerpos intervertebrales vertebrales bajo carga axial Prueba de fatiga cíclica de componentes de bandeja tibial de acuerdo con ASTM F1800 e ISO 14879
Prueba de fatiga cíclica de componentes de bandeja tibial de acuerdo con ASTM F1800 e ISO 14879 Prueba de flexión ISO 16402 de los cementos de resina acrílica utilizados en ortopedia
Prueba de flexión ISO 16402 de los cementos de resina acrílica utilizados en ortopedia ISO 14801 Prueba de fatiga de implantes dentales endoóseos preangulados en un baño de líquidos
ISO 14801 Prueba de fatiga de implantes dentales endoóseos preangulados en un baño de líquidos Pruebas de soportes: materiales de metal, plástico y cerámica
Pruebas de soportes: materiales de metal, plástico y cerámica






